[ 차례 ]
미국
01. 국가 일반 및 바이오의약품 산업 개요
02. 미국 (FDA)의 바이오의약품 분류
03. 바이오의약품 임상시험계획 신청 절차
04. 바이오의약품 품목허가 신청 절차
05. 바이오의약품 심속 심사 제도
유럽
01. 국가 일반 및 바이오의약품 산업 개요
02. 유럽 (EMA)의 바이오의약품 분류
03. 바이오의약품 임상시험계획 신청 절차
04. 바이오의약품 품목허가 신청 절차
05. 바이오의약품 심속 심사 제도
01 국가 일반 및 바이오의약품 산업 개요
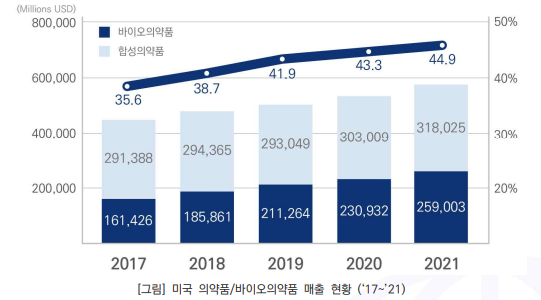
- 미국의 ‘21년 기준 바이오의약품 시장(매출 기준)은 약 2,590억 달러로, 의약품(전체) 대비44.9% 차지함
- 미국 바이오의약품 시장은 최근 5년(’17~‘21)간 연평균 13% 성장함
- 의약품(전체) 대비 바이오의약품 비중은 (’17년) 35.6% → (‘21) 44.9%로 증가함
전체글보기
회원에게만 댓글 작성 권한이 있습니다.